Алканы – предельные углеводороды, их химические свойства. Алканы: строение, номенклатура, изомерия
Предельные углеводороды - это такие соединения, которые представляют собой молекулы, состоящие из атомов углерода, находящихся в состоянии гибридизации sp 3 . Они связаны между собой исключительно ковалентными сигма-связями. Название «предельные» или «насыщенные» углеводороды исходит из того факта, что эти соединения не имеют возможности присоединять какие-либо атомы. Они предельны, полностью насыщены. Исключение составляют циклоалканы.
Что такое алканы?
Алканы - это углеводороды предельные, а их углеродная цепь незамкнута и состоит из атомов углерода, связанных между собой при помощи одинарных связей. Она не содержит иных (то есть двойных, как у алкенов, или же тройных, как у алкилов) связей. Алканы также называют парафинами. Это название они получили, так как общеизвестные парафины являются смесью преимущественно данных предельных углеводородов С 18 -С 35 с особой инертностью.
Общие сведения об алканах и их радикалах
Их формула: С n Р 2 n +2 , здесь n больше или равно 1. Молярная масса вычисляется по формуле: М = 14n + 2. Характерная особенность: окончания в их названиях - «-ан». Остатки их молекул, которые образуются в результате замещения водородных атомов на иные атомы, имеют название алифатических радикалов, или алкилов. Их обозначают буквой R. Общая формула одновалентных алифатических радикалов: С n Р 2 n +1 , здесь n больше или равно 1. Молярная масса алифатических радикалов вычисляется по формуле: М = 14n + 1. Характерная особенность алифатических радикалов: окончания в названиях «-ил». Молекулы алканов имеют свои особенности строения:
- связь С-С характеризуется длиной 0,154 нм;
- связь С-Н характеризуется длиной 0,109 нм;
- валентный угол (угол между связями углерод-углерод) равен 109 градусов и 28 минут.

Начинают гомологический ряд алканы: метан, этан, пропан, бутан и так далее.
Физические свойства алканов
Алканы - это вещества, которые не имеют цвета и нерастворимы в воде. Температура, при которой алканы начинают плавиться, и температура, при которой они закипают, повышаются в соответствии с увеличением молекулярной массы и длины углеводородной цепи. От менее разветвленных к более разветвленным алканам температуры кипения и плавления понижаются. Газообразные алканы способны гореть бледно-голубым либо бесцветным пламенем, при этом выделяется довольно много тепла. СН 4 -С 4 Н 10 представляют собой газы, у которых отсутствует также и запах. С 5 Н 12 -С 15 Н 32 - это жидкости, которые обладают специфическим запахом. С 15 Н 32 и так далее - это твердые вещества, которые также не имеют запаха.
Химические свойства алканов
Данные соединения являются малоактивными в химическом плане, что можно объяснить прочностью трудноразрываемых сигма-связей - С-С и С-Н. Также стоит учитывать, что связи С-С неполярны, а С-Н малополярны. Это малополяризуемые виды связей, относящиеся к сигма-виду и, соответственно, разрываться по наибольшей вероятности они станут по механизму гомолитическому, в результате чего будут образовываться радикалы. Таким образом, химические свойства алканов в основном ограничиваются реакциями радикального замещения.

Реакции нитрования
Алканы взаимодействуют только с азотной кислотой с концентрацией 10% либо с оксидом четырехвалентного азота в газовой среде при температуре 140°С. Реакция нитрования алканов носит название реакции Коновалова. В результате образуются нитросоединения и вода: CH 4 + азотная кислота (разбавленная) = CH 3 - NO 2 (нитрометан) + вода.
Реакции горения
Предельные углеводороды очень часто применяются как топливо, что обосновано их способностью к горению: С n Р 2n+2 + ((3n+1)/2) O 2 = (n+1) H 2 O + n СО 2 .
Реакции окисления
В химические свойства алканов также входит их способность к окислению. В зависимости от того, какие условия сопровождают реакцию и как их изменяют, можно из одного и того же вещества получить различные конечные продукты. Мягкое окисление метана кислородом при наличии катализатора, ускоряющего реакцию, и температуры около 200 °С может дать в результате следующие вещества:
1) 2СН 4 (окисление кислородом) = 2СН 3 ОН (спирт - метанол).
2) СН 4 (окисление кислородом) = СН 2 О (альдегид - метаналь или формальдегид) + Н 2 О.
3) 2СН 4 (окисление кислородом) = 2НСООН (карбоновая кислота - метановая или муравьиная) + 2Н 2 О.

Также окисление алканов может производиться в газообразной или жидкой среде воздухом. Такие реакции приводят к образованию высших жирных спиртов и соответствующих кислот.
Отношение к нагреванию
При температурах, не превышающих +150-250°С, обязательно в присутствии катализатора, происходит структурная перестройка органических веществ, которая заключается в изменении порядка соединения атомов. Данный процесс называется изомеризацией, а вещества, полученные в результате реакции - изомерами. Таким образом, из нормального бутана получается его изомер - изобутан. При температурах 300-600°С и наличии катализатора происходит разрыв связей С-Н с образованием молекул водорода (реакции дегидрирования), молекул водорода с замыканием углеродной цепи в цикл (реакции циклизации или ароматизации алканов):
1) 2СН 4 = С 2 Н 4 (этен) + 2Н 2.
2) 2СН 4 = С 2 Н 2 (этин) + 3Н 2.
3) С 7 Н 16 (нормальный гептан) = С 6 Н 5 - СН 3 (толуол) + 4Н 2 .

Реакции галогенирования
Такие реакции заключаются во введении в молекулу органического вещества галогенов (их атомов), в результате чего образуется связь С-галоген. При взаимодействии алканов с галогенами образуются галогенпроизводные. Данная реакция обладает специфическими особенностями. Она протекает по механизму радикальному, и чтобы ее проинициировать, необходимо на смесь галогенов и алканов воздействовать ультрафиолетовым излучением или же просто нагреть ее. Свойства алканов позволяют реакции галогенирования протекать, пока не будет достигнуто полное замещение на атомы галогена. То есть хлорирование метана не закончится одной стадией и получением метилхлорида. Реакция пойдет далее, будут образовываться все возможные продукты замещения, начиная с хлорметана и заканчивая тетрахлорметаном. Воздействие хлора при данных условиях на другие алканы приведет к образованию различных продуктов, полученных в результате замещения водорода у различных атомов углерода. От температуры, при которой идет реакция, будет зависеть соотношение конечных продуктов и скорость их образования. Чем длиннее углеводородная цепь алкана, тем легче будет идти данная реакция. При галогенировании сначала будет замещаться атом углерода наименее гидрированый (третичный). Первичный вступит в реакцию после всех остальных. Реакция галогенирования будет происходить поэтапно. На первом этапе заместиться только один атом водорода. C растворами галогенов (хлорной и бромной водой) алканы не взаимодействуют.

Реакции сульфохлорирования
Химические свойства алканов также дополняются реакцией сульфохлорирования (она носит название реакции Рида). При воздействии ультрафиолетового излучения алканы способны реагировать со смесью хлора и диоксида серы. В результате образуется хлороводород, а также алкильный радикал, который присоединяет к себе диоксид серы. В результате получается сложное соединение, которое становится стабильным благодаря захвату атома хлора и разрушения очередной его молекулы: R-H + SO 2 + Cl 2 + ультрафиолетовое излучение = R-SO 2 Cl + HCl. Образовавшиеся в результате реакции сульфонилхлориды находят широкое применение в производстве поверхностно-активных веществ.
Строение алканов
Алканы - углеводороды, в молекулах которых атомы связаны одинарными связями и которые соответствуют общей формуле C n H 2n+2 . В молекулах алканов все атомы углерода находятся в состоянии sр 3 -гибридизации .
Это означает, что все четыре гибридные орбитали атома углерода одинаковы по форме, энергии и направлены в углы равносторонней треугольной пирамиды - тетраэдра . Углы между орбиталями равны 109° 28′. Вокруг одинарной углерод-углеродной связи возможно практически свободное вращение, и молекулы алканов могут приобретать самую разнообразную форму с углами при атомах углерода, близкими к тетраэдрическому (109° 28′), например, в молекуле н-пентан.

Особо стоит напомнить о связях в молекулах алканов. Все связи в молекулах предельных углеводородов одинарные. Перекрывание происходит по оси, соединяющей ядра атомов, т. е. это σ-связи . Связи углерод - углерод являются неполярными и плохо поляризуемыми. Длина С-С связи в алканах равна 0,154 нм (1,54 10 10 м). Связи С-Н несколько короче. Электронная плотность немного смещена в сторону более электроотрицательного атома углерода, т. е. связь С-Н является слабополярной .
Гомологический ряд метана
Гомологи - вещества, сходные по строению и свойствам и отличающиеся на одну или более групп СН 2 .


Предельные углеводороды составляют гомологический ряд метана.
Изомерия и номенклатура алканов
Для алканов характерна так называемая структурная изомерия . Структурные изомеры отличаются друг от друга строением углеродного скелета. Простейший алкан, для которого характерны структурные изомеры, - это бутан.
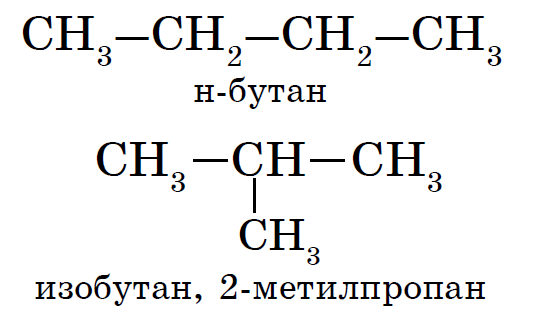
Рассмотрим подробнее для алканов основы номенклатуры ИЮПАК .
1. Выбор главной цепи . Формирование названия углеводорода начинается с определения главной цепи - самой длинной цепочки атомов углерода в молекуле, которая является как бы ее основой.
2. Нумерация атомов главной цепи . Атомам главной цепи присваивают номера. Нумерация атомов главной цепи начинается с того конца, к которому ближе стоит заместитель (структуры А, Б). Если заместители находятся на равном удалении от конца цепи, то нумерация начинается от того конца, при котором их больше (структура В). Если различные заместители находятся на равном удалении от концов цепи, то нумерация начинается с того конца, к которому ближе старший (структура Г). Старшинство углеводородных заместителей определяется по тому, в каком порядке следует в алфавите буква, с которой начинается их название: метил (-СН 3), затем пропил (-СН 2 -СН 2 -СН 3), этил (-СН 2 -СН 3) и т. д.
Обратите внимание на то, что название заместителя формируется заменой суффикса -ан на суффикс -ил в названии соответствующего алкана.
3. Формирование названия . В начале названия указывают цифры - номера атомов углерода, при которых находятся заместители. Если при данном атоме находятся несколько заместителей, то соответствующий номер в названии повторяется дважды через запятую (2,2-). После номера через дефис указывают количество заместителей (ди - два, три - три, тетра - четыре, пента - пять) и название заместителя (метил, этил, пропил). Затем без пробелов и дефисов - название главной цепи. Главная цепь называется как углеводород - член гомологического ряда метана (метан, этан, пропан и т. д.).




Названия веществ, структурные формулы которых приведены выше, следующие:
Структура А: 2-метилпропан;
Структура Б: 3-этилгексан;
Структура В: 2,2,4-триметилпентан;
Структура Г: 2-метил 4-этилгексан.
Отсутствие в молекулах предельных углеводородов полярных связей приводит к тому, что они плохо растворяются в воде , не вступают во взаимодействие с заряженными частицами (ионами) . Наиболее характерными для алканов являются реакции, протекающие с участием свободных радикалов .
Физические свойства алканов
Первые четыре представителя гомологического ряда метана - газы . Простейший из них - метан - газ без цвета, вкуса и запаха (запах «газа», почувствовав который, надо звонить 04, определяется запахом меркаптанов - серосодержащих соединений, специально добавляемых к метану, используемому в бытовых и промышленных газовых приборах для того, чтобы люди, находящиеся рядом с ними, могли по запаху определить утечку).
Углеводороды состава от С 5 Н 12 до С 15 Н 32 - жидкости; более тяжелые углеводороды - твердые вещества. Температуры кипения и плавления алканов постепенно увеличиваются с возрастанием длины углеродной цепи. Все углеводороды плохо растворяются в воде, жидкие углеводороды являются распространенными органическими растворителями.


Химические свойства алканов
Реакции замещения.
Наиболее характерными для алканов являются реакции свободнорадикального замещения , в ходе которого атом водорода замещается на атом галогена или какую-либо группу.
Приведем уравнения характерных реакций галогенирования :
В случае избытка галогена хлорирование может пойти дальше, вплоть до полного замещения всех атомов водорода на хлор :

Полученные вещества широко используются как растворители и исходные вещества в органических синтезах.
Реакция дегидрирования (отщепления водорода).
В ходе пропускания алканов над катализатором (Pt, Ni, Al 2 O 3 , Cr 2 O 3) при высокой температуре (400-600 °C) происходит отщепление молекулы водорода и образование алкена :
Реакции, сопровождающиеся разрушением углеродной цепи. Все предельные углеводороды горят с образованием углекислого газа и воды. Газообразные углеводороды, смешанные с воздухом в определенных соотношениях, могут взрываться.
1. Горение предельных углеводородов - это свободнорадикальная экзотермическая реакция, которая имеет очень большое значение при использовании алканов в качестве топлива:
В общем виде реакцию горения алканов можно записать следующим образом:
2. Термическое расщепление углеводородов .
Процесс протекает по свободнорадикальному механизму . Повышение температуры приводит к гомолитическому разрыву углерод-углеродной связи и образованию свободных радикалов.
Эти радикалы взаимодействуют между собой, обмениваясь атомом водорода, с образованием молекулы алкана и молекулы алкена :
Реакции термического расщепления лежат в основе промышленного процесса - крекинга углеводородов . Этот процесс является важнейшей стадией переработки нефти.
3. Пиролиз . При нагревании метана до температуры 1000 °С начинается пиролиз метана - разложение на простые вещества:
При нагревании до температуры 1500 °С возможно образование ацетилена :
4. Изомеризация . При нагревании линейных углеводородов с катализатором изомеризации (хлоридом алюминия) происходит образование веществ с разветвленным углеродным скелетом :

5. Ароматизация . Алканы с шестью или более углеродными атомами в цепи в присутствии катализатора циклизуются с образованием бензола и его производных:

Алканы вступают в реакции, протекающие по свободнорадикальному механизму, т. к. все атомы углерода в молекулах алканов находятся в состоянии sp 3 -гибридизации. Молекулы этих веществ построены при помощи ковалентных неполярных С-С (углерод - углерод) связей и слабополярных С-Н (углерод - водород) связей. В них нет участков с повышенной и с пониженной электронной плотностью, легко поляризуемых связей, т. е. таких связей, электронная плотность в которых может смещаться под действием внешних факторов (электростатических полей ионов). Следовательно, алканы не будут реагировать с заряженными частицами, т. к. связи в молекулах алканов не разрываются по гетеролитическому механизму.
Ациклические углеводороды называются алканами. Всего насчитывается 390 алканов. Самую длинную структуру имеет нонаконтатриктан (C 390 H 782). К атомам углерода могут присоединяться галогены, образуя галогеналканы.
Строение и номенклатура
По определению алканы - предельные или насыщенные углеводороды, имеющие линейную или разветвлённую структуру. Также называются парафинами. Молекулы алканов содержат только одинарные ковалентные связи между атомами углерода. Общая формула -
Чтобы назвать вещество, необходимо соблюсти правила. По международной номенклатуре названия формируются с помощью суффикса -ан. Названия первых четырёх алканов сложились исторически. Начиная с пятого представителя, названия составляются из приставки, обозначающей количество атомов углерода, и суффикса -ан. Например, окта (восемь) образует октан.
Для разветвлённых цепей названия складываются:
- из цифр, указывающих номера атомов углерода, около которых стоят радикалы;
- из названия радикалов;
- из названия главной цепи.
Пример: 4-метилпропан - у четвёртого атома углерода в цепи пропана находится радикал (метил).

Рис. 1. Структурные формулы с названиями алканов.
Каждый десятый алкан даёт называние следующим девяти алканам. После декана идут ундекан, додекан и далее, после эйкозана - генэйкозан, докозан, трикозан и т.д.
Гомологический ряд
Первый представитель - метан, поэтому алканы также называют гомологическим рядом метана. В таблице алканов указаны первые 20 представителей.
|
Название |
Формула |
Название |
Формула |
|
Тридекан |
|||
|
Тетрадекан |
|||
|
Пентадекан |
|||
|
Гексадекан |
|||
|
Гептадекан |
|||
|
Октадекан |
|||
|
Нанадекан |
|||
Начиная с бутана, все алканы имеют структурные изомеры. К названию прибавляется приставка изо-: изобутан, изопропан, изогексан.

Рис. 2. Примеры изомеров.
Физические свойства
Агрегатное состояние веществ меняется в списке гомологов сверху вниз. Чем больше содержится атомов углерода и, соответственно, чем больше молекулярная масса соединений, тем выше температура кипения и твёрже вещество.
Остальные вещества, содержащие больше 15 атомов углерода, находятся в твёрдом состоянии.

Газообразные алканы горят голубым или бесцветным пламенем.
Получение
Алканы, как и другие классы углеводородов, получают из нефти, газа, каменного угля. Для этого используют лабораторные и промышленные методы:
- газификация твёрдого топлива:
C + 2H 2 → CH 4 ;
- гидрирование оксида углерода (II):
CO + 3H 2 → CH 4 + H 2 O;
- гидролиз карбида алюминия:
Al 4 C 3 + 12H 2 O → 4Al(OH) 3 + 3CH 4 ;
- реакция карбида алюминия с сильными кислотами:
Al 4 C 3 + H 2 Cl → CH 4 + AlCl 3 ;
- восстановление галогеналканов (реакция замещения):
2CH 3 Cl + 2Na → CH 3 -CH 3 + 2NaCl;
- гидрирование галогеналканов:
CH 3 Cl + H 2 → CH 4 + HCl;
- сплавление солей уксусной кислоты со щелочами (реакция Дюма):
CH 3 COONa + NaOH → Na 2 CO 3 + CH 4 .
Алканы можно получить гидрированием алкенов и алкинов в присутствии катализатора - платины, никеля, палладия.
Химические свойства
Алканы вступают в реакции с неорганическими веществами:
- горение:
CH 4 + 2O 2 → CO 2 + 2H 2 O;
- галогенирование:
CH 4 + Cl 2 → CH 3 Cl + HCl;
- нитрирование (реакция Коновалова):
CH 4 + HNO 3 → CH 3 NO 2 + H 2 O;
- присоединение:
Алканами называют насыщенные углеводороды. В их молекулах атомы имеют одинарные связи. Структура определяется формулой CnH2n+2. Рассмотрим алканы: химические свойства, виды, применение.
В структуре углерода есть четыре орбиты, по которым вращаются атомы. Орбитали обладают одинаковой формой, энергией.
Обратите внимание! Углы между ними составляют 109 градусов и 28 минут, они направлены на вершины тетраэдра.
Простая углеродная связь позволяет алкановым молекулам свободно вращаться, в результате чего структуры приобретают различные формы, образуя вершины при атомах углерода.
Все алкановые соединения разделяются на две основные группы:
- Углеводороды алифатического соединения. Такие структуры обладают линейным соединением. Общая формула выглядит таким образом: CnH2n+2. Значение n равно или больше единицы, означает количество углеродных атомов.
- Циклоалканы циклической структуры. Химические свойства циклических алканов значительно отличаются от свойств линейных соединений. Формула циклоалканов в некоторой степени делает их схожими с углеводородами, обладающими тройной атомной связью, то есть с алкинами.
Виды алканов
Существует несколько видов алкановых соединений, каждой из которых имеет свою формулу, строение, химические свойства и алкильный заместитель. Таблица содержит гомологический ряд

Название алканов
Общая формула насыщенных углеводородов — CnH2n+2. Изменяя значение n, получают соединение с простой межатомной связью.
Полезное видео: алканы — строение молекул, физические свойства
Разновидности алканов, варианты реакций
В естественных условиях алканы являются химически инертными соединения. Углеводороды не реагируют на контактирование с концентратом азотной и серной кислоты, щелочью и перманганатом калия.
Одинарные молекулярные связи определяют реакции, характерные для алканов. Алкановые цепочки отличаются неполярной и слабо поляризуемой связью. Она несколько длиннее, нежели С-Н.

Общая формула алканов
Реакция замещения
Парафиновые вещества отличаются незначительной химической активностью. Объясняется это повышенной прочностью цепной связи, которую непросто разорвать. Для разрушения используют гомологический механизм, в котором принимают участие свободные радикалы.
Для алканов более естественны реакции замещения. Они не реагируют на молекулы воды и заряженные ионы. При замещении происходит замена водородных частиц галогеновыми и прочими активными элементами. Среди подобных процессов выделяют галогенирование, нитрирование и сульфохлорирование. Такие реакции используют для образования алкановых производных.
Свободнорадикальное замещение происходит в три основных этапа:
- Появление цепочки, на основе которой создаются свободные радикалы. В качестве катализаторов используют нагревание и ультрафиолетовый свет.
- Развитие цепочки, в структуре которой происходят взаимодействия активных и неактивных частиц. Так формируются молекулы и радикальные частицы.
- В завершение цепочка обрывается. Активные элементы создают новые комбинации или вовсе исчезают. Цепная реакция завершается.
Галогенирование
Процесс осуществляется по радикальному типу. Галогенирование происходит под воздействием ультрафиолета и температурного нагрева углеводородной и галогеновой смеси.
Весь процесс происходит по правилу Марковникова. Суть его заключается в том, что первым галогенированию подвергается атом водорода, принадлежащий гидрированному углероду. Процесс начинается с третичного атома и заканчивается первичным углеродом.
Сульфохлорирование
Другое название – реакция Рида. Осуществляется она методом свободнорадикального замещения. Таким образом, алканы реагируют на действие комбинации серного диоксида и хлора под воздействием ультрафиолетового излучения.
Реакция начинается с активизации цепного механизма. В это время из хлора выделяются два радикала. Действие одного направлено на алкан, в результате формируется молекула хлорводорода и алкильный элемент. Другой радикал соединяется с диоксидом серы, создавая сложную комбинацию. Для равновесия из другой молекулы отбирают один атом хлора. В итоге получают сульфонилхлорид алкана. Это вещество используют для выработки поверхностно-активных компонентов.

Сульфохлорирование
Нитрование
Процесс нитрования подразумевает соединение насыщенных углеродов с газообразным оксидом четырехвалентного азота и азотной кислотой, доведенной до 10% раствора. Для протекания реакции потребуется низкий уровень давления и высокая температура, приблизительно 104 градуса. В результате нитрования получают нитроалканы.
Отщепление
Посредством отделения атомов проводят реакции дегидрирования. Молекулярная частица метана полностью разлагается под влиянием температуры.
Дегидрирование
Если от углеродной решетки парафина (кроме метана) отделить атом водорода, образуются непредельные соединения. Эти реакции осуществляются в условиях значительных температурных режимов (400-600 градусов). Также используются различные металлические катализаторы.
Получение алканов происходит путем проведения гидрирования непредельных углеводородов.
Процесс разложения
При влиянии температур во время алкановых реакций могут происходить разрывы молекулярных связей, выделение активных радикалов. Эти процессы известны под названием пиролиз и крекинг.
При нагревании реакционного компонента до 500 градусов, молекулы начинают разлагаться, а на их месте формируются сложные радикальные алкильные смеси. Таким способом получают алканы и алкены в промышленности.
Окисление
Это химические реакции, основанные на отдаче электронов. Для парафинов характерно автоокисление. В процессе используется окисление насыщенных углеводородов свободными радикалами. Алкановые соединения в жидком состоянии преобразуются в гидроперекись. Сначала парафин вступает в реакцию с кислородом. Образуются активные радикалы. Затем происходит реакция алкильной частицы со второй молекулой кислорода. Формируется перекисный радикал, который в последствие взаимодействует с алкановой молекулой. В результате процесса выделяется гидроперекись.

Реакция окисления алканов
Применение алканов
Углеродные соединения имеют широкое применение практически во всех основных сферах человеческой жизни. Некоторые из видов соединений являются незаменимыми для определенных отраслей производства и комфортного существования современного человека.
Газообразные алканы – основа ценного топлива. Главным компонентом большинства газов является метан.
Метан обладает способностью создавать и выделять большое количество тепла. Поэтому его в значительных объемах применяют в промышленности, для потребления в бытовых условиях. При смешивании бутана и пропана получают хорошее бытовое топливо.
Метан используют при производстве таких продуктов:
- метанол;
- растворители;
- фреон;
- типографская краска;
- топливо;
- синтез-газ;
- ацетилен;
- формальдегид;
- муравьиная кислота;
- пластмасса.

Применение метана
Жидкие углеводороды предназначены для создания топлива для двигателей и ракет, растворителей.
Высшие углеводороды, где количество атомов углерода превышает 20, участвуют в производстве смазочных веществ, лакокрасочной продукции, мыла и моющих средств.
Комбинация жирных углеводородов, в которых менее 15 атомов Н, являет собой вазелиновое масло. Эта безвкусная прозрачная жидкость применяется в косметике, в создании парфюмов, в медицинских целях.
Вазелин – результат соединения твердых и жирных алканов с количеством атомов углерода меньше 25. Вещество участвует в создании медицинских мазей.
Парафин, полученный в результате комбинирования твердых алканов, является твердой безвкусной массой, белого цвета и без аромата. Из вещества производят свечи, пропитывающую субстанцию для упаковочной бумаги и спичек. Также парафин популярен при осуществлении тепловых процедур в косметологии и медицине.
Обратите внимание! На основе алкановых смесей также делают синтетические волокна, пластмассы, моющую химию и каучук.
Галогенопроизводные алкановые соединения выполняют функции растворителей, хладагентов, а также основного вещества для дальнейшего синтеза.
Полезное видео: алканы — химические свойства
Вывод
Алканы являются ациклическими углеводородными соединениями, обладающими линейной или разветвленной структурой. Между атомами установлена одинарная связь, которая не поддается разрушению. Реакции алканов, основанные на замещении молекул, свойственные этому виду соединений. Гомологический ряд имеет общую структурную формулу CnH2n+2. Углеводороды относятся к насыщенному классу, поскольку содержат максимально допустимое количество атомов водорода.
Алканы :
Алканы - это предельные углеводороды, в молекулах которых все атомы связаны одинарными связями. Формула -
Физические свойства :
- Температуры плавления и кипения увеличиваются с молекулярной массой и длиной главной углеродной цепи
- При нормальных условиях неразветвлённые алканы с CH 4 до C 4 H 10 - газы; с C 5 H 12 до C 13 H 28 - жидкости; после C 14 H 30 - твёрдые тела.
- Температуры плавления и кипения понижаются от менее разветвленных к более разветвленным. Так, например, при 20 °C н-пентан - жидкость, а неопентан - газ.
Химические свойства:
· Галогенирование
это одна из реакций замещения. В первую очередь галогенируется наименее гидрированый атом углерода (третичный атом, затем вторичный, первичные атому галогенируются в последнюю очередь). Галогенирование алканов проходит поэтапно - за один этап замещается не более одного атома водорода:
- CH 4 + Cl 2 → CH 3 Cl + HCl (хлорметан)
- CH 3 Cl + Cl 2 → CH 2 Cl 2 + HCl (дихлорметан)
- CH 2 Cl 2 + Cl 2 → CHCl 3 + HCl (трихлорметан)
- CHCl 3 + Cl 2 → CCl 4 + HCl (тетрахлорметан).
Под действием света молекула хлора распадается на радикалы, затем они атакуют молекулы алкана, забирая у них атом водорода, в результате этого образуются метильные радикалы ·СН 3 , которые сталкиваются с молекулами хлора, разрушая их и образуя новые радикалы.
· Горение
Основным химическим свойством предельных углеводородов, определяющих их использование в качестве топлива, является реакция горения. Пример:
CH 4 + 2O 2 → CO 2 + 2H 2 O + Q
В случае нехватки кислорода вместо углекислого газа получается угарный газ или уголь (в зависимости от концентрации кислорода).
В общем виде реакцию горения алканов можно записать следующим образом:
С n Н 2n +2 +(1,5n +0,5)O 2 = n CO 2 + (n +1)H 2 O
· Разложение
Реакции разложения происходят лишь под влиянием больших температур. Повышение температуры приводит к разрыву углеродной связи и образованию свободных радикалов.
Примеры:
CH 4 → C + 2H 2 (t > 1000 °C)
C 2 H 6 → 2C + 3H 2
Алкены :
Алкены-это непредельные углеводороды,содержащие в молекуле,кроме одинарных связей,одну двойную углерод-углеродную связь.Формула- C n H 2n
Принадлежность углеводорода к классу алкенов отражают родовым суффиксом –ен в его названии.
Физические свойства :
- Температуры плавления и кипения алкенов (упрощенно) увеличиваются с молекулярной массой и длиной главной углеродной цепи.
- При нормальных условиях алкены с C 2 H 4 до C 4 H 8 - газы; с C 5 H 10 до C 17 H 34 - жидкости, после C 18 H 36 - твёрдые тела. Алкены не растворяются в воде, но хорошо растворяются в органических растворителях.
Химические свойства :
· Дегидратация -это процесс отщепления молекулы воды от молекулы органического соединения.
· Полимеризация -это химический процесс соединения множества исходных молекул низкомолекулярного вещества в крупные молекулы полимера.
Полимер -это высокомолекулярное соединение,молекулы которого состоят из множества одинаковых структурных звеньев.
Алкадиены :
Алкадиены -это непредельные углеводороды, содержащие в молекуле,кроме одинрных связей,дведвойные углерод-углеродные связи.Формула-
. Диены являются структурными изомерамиалкинов.Физические свойства :
Бутадие́н - газ (tкип −4,5 °C), изопрен - жидкость, кипящая при 34 °C, диметилбутадиен - жидкость, кипящая при 70 °C. Изопрен и другие диеновые углеводороды способны полимеризоваться в каучук. Натуральный каучук в очищенном состоянии является полимером с общей формулой (С5Н8)n и получается из млечного сока некоторых тропических растений.
Каучук хорошо растворим в бензоле, бензине, сероуглероде. При низкой температуре становится ломким, при нагревании липким. Для улучшения механических и химических свойств каучука его превращают в резину, подвергая вулканизации. Для получения резиновых изделий сначала их формуют из смеси каучука с серой, а также с наполнителями: сажей, мелом, глиной и некоторыми органическими соединениями, служащими для ускорения вулканизации. Затем изделия нагревают - горячая вулканизация. При вулканизации сера химически связывается с каучуком. Кроме того, в вулканизированном каучуке сера содержится в свободном состоянии в виде мельчайших частиц.
Диеновые углеводороды легко полимеризуются. Реакция полимеризации диеновых углеводородов лежит в основе синтеза каучука. Вступают в реакции присоединения (гидрирование, галогенирование, гидрогалогенирование):
H 2 C=CH-CH=CH 2 + H 2 -> H 3 C-CH=CH-CH 3
Алкины :
Алкины-этонепредельные углеводороды молекулы которых содержат,помимо одинарных связей,одну тройную углерод-глеродную связь.Формула-C n H 2n-2
Физические свойства :
Алкины по своим физическим свойствам напоминают соответствующие алкены. Низшие (до С 4) - газы без цвета и запаха, имеющие более высокие температуры кипения, чем аналоги в алкенах.
Алкины плохо растворимы в воде, лучше - в органических растворителях.
Химические свойства :
· Реакции галогенирования
Алкины способны присоединять одну или две молекулы галогена с образованием соответствующих галогенпроизводных:
· Гидратация
В присутствии солей ртути алкины присоединяют воду с образованием ацетальдегида (для ацетилена) или кетона (для прочих алкинов)





